Oxydativer Stress fördert die Bildung von H2O2
Oxydativer Stress fördert die Bildung von Wasserstoffperoxyd (H2O2). Immunzellen setzten infolge von Entzündungsreaktionen dieses Molekül in Entzündungsgebieten in hohem Maße frei. Dieses Molekül scheint einen wesentlichen Einfluss auf die normale Glucoseverwertung der Zelle zu nehmen. Unter normalen Bedingungen wird Glucose in der aeroben Glycolyse zur Energiegewinnung verbrannt. Die maximale Energieausbeute pro Mol Glucose liegt bei 38 Mol ATP. Diese Glucoseverwertung wird unter oxydativem Stress sehr schnell blockiert.
H2O2 fördert den Glucoseabbau über den Pentosephosphatzyklus
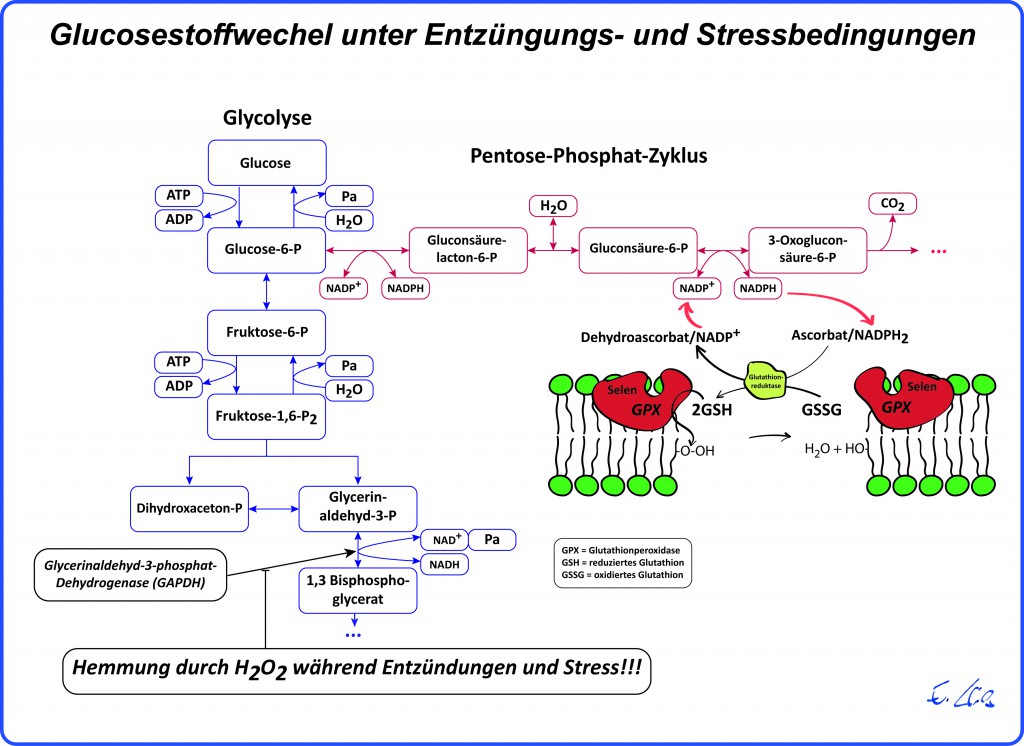
Das Schlüsselenzym Glycerinaldehyd-3-Phosphat-Dehydrogenase (GAPDH) wird wesentlich durch den hohen H2O2 Gehalt blockiert, so dass kein weiterer Abbau in der Glycolyse möglich ist. Alternativ muss die Glucose einen Abbauweg beschreiten, der für die Zelle einen enormen Schutz vor dem hohen H2O2 Spiegel darstellt. Der Abbau über den Pentosephosphatzyklus (PPZ) liefert das notwendige Redoxcoenzym NADPH2 (reduziertes Nicotinamid-Adenin-Dinukleotid-Phosphat), das indirekt für die Regeneration der Glutathionperoxidase benötigt wird. Der Mechanismus ist relativ komplex und kann hier nur angedeutet werden. Die Glutathionperoxydase ist maßgeblich am Abbau von Wasserstoffperoxyd und anderen Peroxyden beteiligt. Dabei überträgt sie Elektronen und Wasserstoff vom reduzierten Glutathion (2 x GSH) auf Peroxyde, so dass Wasser und ein unproblematischer Alkoholrest entstehen. Dabei entsteht allerdings oxydiertes Glutathion (GSSG), dass in einem Glutathionreduktase katalysierten Schritt in die reduzierte Form wieder überführt werden muss. Der Wasserstoff- und Elektronendonator ist hierbei NADPH2, das im PPZ gebildet wird. Somit reguliert ein hoch reaktives, zellschädigendes Sauerstoffagens den Glucosestoffwechsel der geschädigten Zellen in dem Maße, dass es die Zelle vor Oxydation der Zellmembran und DNA schütz und somit deren Überleben sichert.
Antioxydative Verbindungen nehmen Einfluss auf den H2O2 Gehalt der Zelle
Anhand dieser Steuerung lässt sich gut verstehen, wie sinnvoll die Evolution zelluläre Prozesse gesteuert hat. Feinste Regulationsmechanismen entstehen als Antwort auf sich verändernde Metabolitkonzentrationen. Wie effektiv insbesondere der oben beschriebene Regulationsmechanismus ist, lässt sich daran erkennen, dass die GAPDH in fast allen Lebewesen (vom Bakterium bis zum Menschen) sehr effektiv durch H2O2 gesteuert wird. Alles deutet darauf hin, dass diese Regulation für das Überleben unter Stressbedingungen eine entscheidende Rolle spielt.
Welche Auswirkungen unsere veränderte Ernährung auf diesen komplexen Mechanismus hat, ist noch sehr unklar. Grundsätzlich sollte in Betracht gezogen werden, dass die hohe Aufnahme antioxidativer Substanzen wie Vitamin C, E, beta-Carotin, die unnötig jedem Lebensmittel zugesetzt werden, den Zellen einen gewissen Schutz ermöglicht. Andererseits wird das regulative Wasserstoffperoxydsystem dadurch nachhaltig gestört, so dass ggf. Regulationsmechanismen nun nicht mehr greifen, die schneller zu einem Zelluntergang führen können.
Quelle: David Peralta et al. (2015). A proton relay enhances H2O2 sensitivity of GADPH to facilitate metabolic adaptation. Nature Chemical Biology 2015, DOI: 10.1038/nchembio.1720
Wir hoffen, dass euch der Artikel über die Glukosestoffwechselregulation gefallen hat. Die Inhalte dieses Artikels sind auch Teil der Diätassistentenausbildung an unserer Schule. Wenn ihr Interesse bekommen habt besucht doch unsere Homepage unter www.bfsdiät.de und informiert euch über diese Ausbildung. Alles Gute und bis zum nächsten Artikel.
